Elementos representativos e transição
Outra forma de classificar os elementos é dividindo-os em elementos representativos e de transição conforme a distribuição eletrônica do átomo.
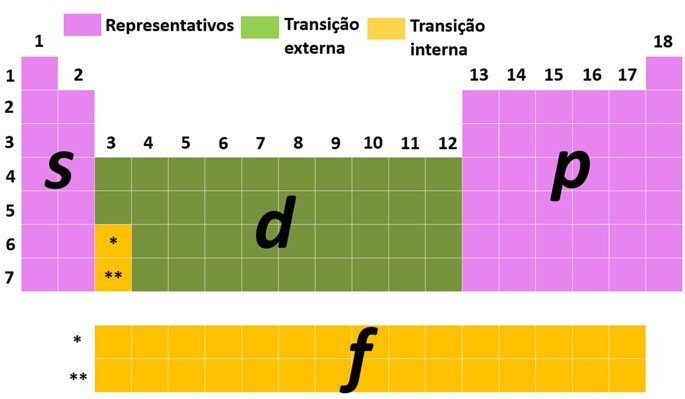
Elementos Representativos
Os elementos representativos são aqueles que apresentam a configuração eletrônica terminada com o subnível mais energético em s (grupos 1 e 2) ou p (grupos 13, 14, 15, 16, 17 e 18).

Os elementos representativos apresentam um comportamento químico relativamente menos complexo que os elementos de transição e formam a maioria das substâncias que nos rodeiam.
Algumas das famílias de elementos representativos recebem nomes especiais, conforme vemos a seguir:
|
Grupo |
Família | Nome específico | Origem do nome | Elementos | Configuração eletrônica |
|---|---|---|---|---|---|
| 1 | 1A | Metais alcalinos | Do latim alcali, que significa “cinza de plantas”. | Li, Na, K, Rb, Cs e Fr |
ns1 |
| 2 | 2A | Metais alcalinoterrosos | O termo "terroso" refere-se a "existir na terra". | Be, Mg, Ca, Sr, Ba e Ra |
ns2 |
| 13 | 3A | Família do Boro | Nome do primeiro elemento da família. | B, Al, Ga, In, Tl e Nh. | ns2np1 |
| 14 | 4A | Família do Carbono | Nome do primeiro elemento da família. | C, Si, Ge, Sn, Pb e Fl. | ns2np2 |
| 15 | 5A | Família do Nitrogênio | Nome do primeiro elemento da família. | N, P, As, Sb, Bi e Mc. | ns2np3 |
| 16 | 6A | Calcogênios | Do grego khalkós, pois são elementos encontrados em minérios de cobre. | O, S, Se, Te, Po e Lv. | ns2np4 |
| 17 | 7A | Halogênios | Expressão grega que significa formadores de sais. | F, Cl, Br, I, At e Ts. | ns2np5 |
| 18 | 0 | Gases Nobres | Considerava-se que não reagia com outras substâncias. | He, Ne, Ar, Kr, Xe, Re e Og. |
1s2 (He) ou ns2np6 |
Através da tabela, podemos observar que:
- Os elementos apresentados acima são classificados em representativos por apresentarem o elétron mais energético em um subnível s ou p.
- Os elétrons distribuem-se por níveis de energia e n representa o nível mais externo do átomo no estado fundamental.
- Os elementos representativos, segundo a recomendação da IUPAC, pertencem aos grupos ou famílias 1,2,13,14,15,16,17 e 18.
O hidrogênio é classificado à parte dos outros elementos. Mesmo possuindo configuração eletrônica 1s1, ele não faz parte do grupo 1 por apresentar um comportamento singular.
Elementos de transição

Os elementos de transição correspondem aos grupos de 3 a 12. Recebem esse nome por possuírem características intermediárias entre os grupos 1 e 2 e os elementos representativos não metálicos.
Os metais de transição são definidos pela IUPAC como:
Um elemento de transição possui um subnível d incompleto ou pode formar cátions com um subnível d incompleto.
Quando o elétron mais energético do átomo no estado fundamental está em um subnível d incompleto, ele é caracterizado como de transição externa.
Os lantanídeos e os actinídeos são elementos de transição interna por possuir ao menos um subnível f incompleto.
Quando os elementos têm elétrons que preenchem os orbitais d ou f, eles exibem propriedades semelhantes e podem ser classificados em elementos de transição externa ou interna.
Como observamos na imagem, a família 8B corresponde a 3 colunas, são os grupos 8, 9 e 10, que foram agrupados assim por ter características próximas.


