Entropia
Entropia é a medida do grau de desordem de um sistema, sendo uma medida da indisponibilidade da energia.
É uma grandeza física que está relacionada com a Segunda Lei da Termodinâmica e que tende a aumentar naturalmente no Universo.
Significado de Entropia
A “desordem” não deve ser compreendida como “bagunça” e sim como a forma de organização de sistema.
O conceito de entropia às vezes é aplicado em outras áreas de conhecimento com esse sentido de desordem, que mais se aproxima do senso comum.
Por exemplo, vamos imaginar três potes, um com pequenas bolinhas azuis, outro com o mesmo tipo de bolinhas só que vermelhas e o terceiro vazio.
Pegamos o pote vazio e colocamos por baixo todas as bolas azuis e por cima todas as bolas vermelhas. Neste caso, as bolas estão separadas e organizadas pela cor.
Ao balançar o pote, as bolinhas começaram a se misturar de forma que num dado momento não existe mais a separação inicial.
Mesmo que continuemos a balançar o pote, dificilmente as bolinhas voltarão a ficar na mesma organização inicial. Ou seja, o sistema ordenado (bolinhas separadas por cor) se tornou um sistema desordenado (bolinhas misturadas).
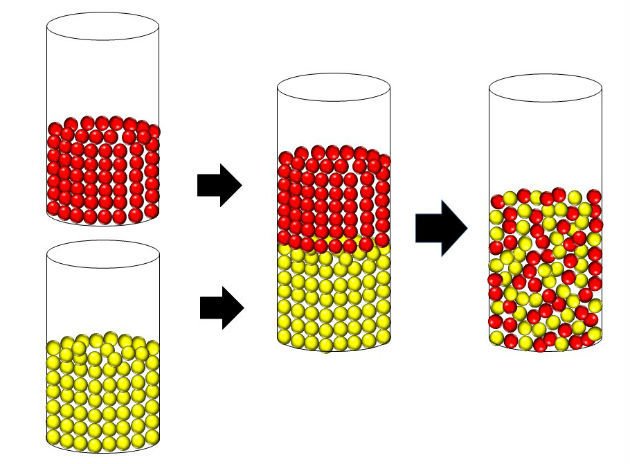
Desse modo, a tendência natural é de aumentar a desordem de um sistema, o que significa um aumento da entropia. Podemos dizer então que nos sistemas: ΔS >0, onde S é entropia.
Entenda também o que é Entalpia.
Entropia e Termodinâmica
O conceito de Entropia começou a ser desenvolvido pelo engenheiro e pesquisador francês Nicolas Sadi Carnot.
Em suas pesquisas sobre transformação da energia mecânica em térmica, e vice-versa, ele constatou que seria impossível que existisse uma máquina térmica com eficiência total.
A Primeira Lei da Termodinâmica determina, basicamente, que "a energia se conserva". Isso quer dizer que nos processos físicos a energia não se perde, ela se converte de um tipo em outro.
Por exemplo, uma máquina utiliza energia para realizar trabalho e nesse processo a máquina aquece. Ou seja, a energia mecânica está sendo degradada em energia térmica.
A energia térmica não se transforma novamente em energia mecânica (se isso acontecesse a máquina nunca deixaria de funcionar), portanto, o processo é irreversível.
Mais tarde, o Lord Kelvin complementou as pesquisas de Carnot sobre a irreversibilidade dos processos termodinâmicos, dando origem às bases da Segunda Lei da Termodinâmica.
Rudolf Clausius foi o primeiro a usar o termo Entropia em 1865. A entropia seria a medida da quantidade de energia térmica que não pode ser revertida em energia mecânica (não pode realizar trabalho), em uma determinada temperatura.
Clausius desenvolveu a fórmula matemática para a variação da entropia (ΔS) que é utilizada atualmente.
![]()
Sendo,
ΔS: variação da entropia (J/K)
Q: calor transferido (J)
T: temperatura (K)
Leia também:
Exercícios Resolvidos
1) Enem - 2016
Até 1824 acreditava-se que as máquinas térmicas, cujos exemplos são as máquinas a vapor e os atuais motores a combustão, poderiam ter um funcionamento ideal. Sadi Carnot demonstrou a impossibilidade de uma máquina térmica, funcionando em ciclos entre duas fontes térmicas (uma quente e outra fria), obter 100% de rendimento. Tal limitação ocorre porque essas máquinas
a) realizam trabalho mecânico.
b) produzem aumento da entropia.
c) utilizam transformações adiabáticas.
d) contrariam a lei da conservação de energia.
e) funcionam com temperatura igual à da fonte quente.
2) Enem - 2011
Um motor só poderá realizar trabalho se receber uma quantidade de energia de outro sistema. No caso, a energia armazenada no combustível é, em parte, liberada durante a combustão para que o aparelho possa funcionar. Quando o motor funciona, parte da energia convertida ou transformada na combustão não pode ser utilizada para a realização de trabalho. Isso significa dizer que há vazamento da energia em outra forma. Carvalho, A. X. Z.
Física Térmica. Belo Horizonte: Pax, 2009 (adaptado).
De acordo com o texto, as transformações de energia que ocorrem durante o funcionamento do motor são decorrentes de a
a) liberação de calor dentro do motor ser impossível.
b) realização de trabalho pelo motor ser incontrolável.
c) conversão integral de calor em trabalho ser impossível.
d) transformação de energia térmica em cinética ser impossível.
e) utilização de energia potencial do combustível ser incontrolável.
Veja também: Exercícios sobre Termodinâmica
GOUVEIA, Rosimar. Entropia. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/entropia/. Acesso em:


