Éster: o que é, nomenclatura, exemplos e para que serve
Ésteres são compostos orgânicos derivados dos ácidos carboxílicos, pois são produzidos a partir de uma reação de esterificação entre um ácido carboxílico e um álcool.
Os ésteres possuem um radical carbônico no lugar do hidrogênio dos carboxílicos, sendo essa a característica que distingue um do outro. O grupo funcional dessa função orgânica oxigenada é R—COO—R’.
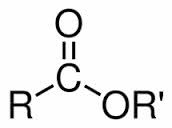
O Éster não é solúvel em água, mas sim em solventes orgânicos, como álcool, éter e clorofórmio. O ponto de ebulição do éster é menor do que o dos álcoois.
São exemplos de ésteres: butanoato de etila (aroma de morango), etanoato de butila (aroma de maçã verde), etanoato de etila (aroma de maçã), etanoato de propila (aroma de pera).
Nomenclatura dos ésteres
Segundo a IUPAC (União Internacional de Química Pura e Aplicada, em português), a nomenclatura dos ésteres deve ser feita da seguinte forma:
- Prefixo: indica o número de carbonos;
- Intermédio: indica o tipo de ligação química;
- Sufixo: -oato é acrescentado, tal como o elemento “de”;
- Terminação: segue-se a terminação -ila.
Por exemplo, o butanoato de etila é um éster que confere o aroma de abacaxi.
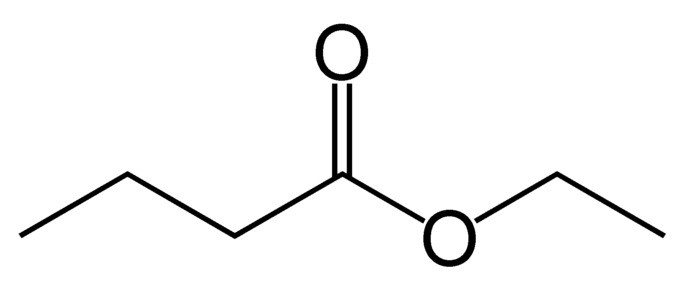 A estrutura de seu nome é:
A estrutura de seu nome é:
- Prefixo et: 2 carbonos
- Intermédio an: ligações simples
- Acréscimo da partícula “oato”
- Ligação de
- Radical etil
- Sufixo = ila
Saiba mais em Funções Orgânicas.
Reação de esterificação
A esterificação é uma reação química que produz éster e água quando um ácido carboxílico e um álcool reagem entre si.
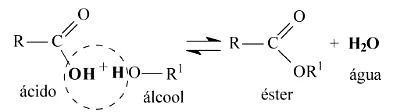
Genericamente, a reação é representada da seguinte forma:
ÁCIDO CARBOXÍLICO + ÁLCOOL → ÉSTER + ÁGUA
A água (H2O) é formada pela união do hidroxila (OH) do ácido carboxílico com o hidrogênio (H) do álcool. A cadeia carbônica do ácido e do álcool se unem para formar a estrutura do éster.
Por ser uma reação lenta, a velocidade da reação pode ser aumentada ao elevar a temperatura e utilizar um catalisador. O processo mais conhecido para produção industrial de ésteres é a Esterificação de Fischer.
A reação de esterificação é lenta, sendo necessário um aumento de temperatura e a presença de um catalisador para acelerar a sua velocidade. Esse processo é denominado de Esterificação de Fischer.
A reação inversa a uma esterificação recebe o nome de hidrólise de éster. Portanto, a partir de éster e água são produzidos ácido carboxílico e álcool.
Leia também sobre transesterificação.
Para que servem os ésteres?
Os ésteres possuem cheiro e aroma agradáveis, daí decorre a sua principal aplicação. Eles são substâncias flavorizantes, ou seja, são utilizados para aromatizar artificialmente coisas como balinhas, sucos e xaropes.
Esses compostos aromatizantes são utilizados em alimentos, mas existem também os triglicerídeos que são triésteres presentes em óleos e gorduras.
O éster também consta na composição do biodiesel. A partir dos ésteres, ainda, surge o sabão. Isso porque óleos e gorduras presentes podem ser usados na sua fabricação.
Saiba mais sobre as funções orgânicas com os conteúdos:
Referências Bibliográficas
Bruice, P. Y.; Química Orgânica - vol. 1 e 2, 4ª ed., Pearson - Prentice Hall, São Paulo, 2006.
CAREY, F. A.; Química Orgânica, 7ª ed., vol. 1 e 2, AMGH Editora Ltda, Porto Alegre, 2011.
MORRISOM, R., BOYD, R., Química Orgânica, 8ª Edição, Fundação Calouste Gulbenkian; Lisboa, 1985.
BATISTA, Carolina. Éster: o que é, nomenclatura, exemplos e para que serve. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/esteres/. Acesso em:


