Exercício sobre reações químicas (com gabarito resolvido)
Sempre que um fenômeno químico ocorre, podemos dizer que ocorre uma reação química.
As reações químicas são representadas por equações químicas: reagentes → produtos.
Estudar sobre as reações químicas é fundamental para entender as transformações que ocorrem no universo e a compreensão da natureza.
Desenvolva seus conhecimentos sobre o tema com as 7 questões a seguir.
Questão 1
O nitrato de amônio (NH4NO3) é um fertilizante essencial para a agricultura, pois fornece nitrogênio que melhora o crescimento das plantas e a produtividade das lavouras. Ele é obtido industrialmente pela reação a seguir:
HNO3 + NH3 → NH4NO3
A reação de produção desse fertilizante, é classificada como:
a) síntese
b) decomposição
c) simples troca
d) dupla troca
e) combustão
a) Síntese
Observe que a equação tem dois reagentes se unindo para sintetizar um único produto, por isso, é uma reação de síntese ou adição.
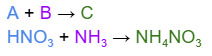
Questão 2
O ácido carbônico (H2CO3) é um ácido fraco que está presente em bebidas carbonatadas e nos processos fisiológicos, como a regulação do pH sanguíneo. Por ser um ácido instável, ele reage para formar água e gás carbônico:
H2CO3(aq) → H2O(l) + CO2 (g).
Identifique o tipo de reação envolvida na equação.
a) adição
b) decomposição
c) deslocamento
d) dupla troca
e) precipitação
b) decomposição
Pela equação, percebe-se que tem um reagente se decompondo em dois produtos, por isso, é uma reação do tipo decomposição ou análise.
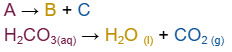
Questão 3
Quando um ácido reage com um metal, forma-se um sal e libera-se gás hidrogênio (H2). Um exemplo é a reação do ácido clorídrico (HCl) com o zinco (Zn):
Zn + 2HCl → ZnCl2 + H2(g). Esse processo é comum na produção de hidrogênio e na corrosão de metais.
Com base na equação apresentada, identifique o tipo de reação que está ocorrendo.
a) adição
b) análise
c) simples troca
d) dupla troca
e) combustão
c) simples troca
Observando a reação, percebe-se dois reagentes: uma substância simples + uma substância composta
Lembre-se: substância simples é aquela formada por apenas um elemento.
Substância composta é formada por dois ou mais elementos.
A reação formada por subst. simples + subst. composta é a reação de simples troca.
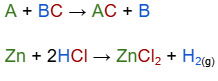
Questão 4
A azia é um um excesso de ácido no estômago, que pode ser neutralizado ao tomar bicarbonato de sódio. A reação entre o bicarbonato e o ácido do estômago alivia a acidez e a sensação de queimação. Como mostra a equação:
NaHCO3 + HCl → NaCl + H2CO3.
Com base na equação apresentada, identifique o tipo de reação que está ocorrendo.
a) síntese
b) decomposição
c) deslocamento
d) dupla troca
e) combustão
d) dupla troca
Pela reação química apresentada, nota-se a presença de dois reagentes: duas substâncias compostas, o que é característico de reações do tipo dupla troca.
Lembre-se: substância composta é formada por dois ou mais elementos.
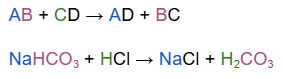
Questão 5
Assinale a sequência que corresponde, respectivamente, às reações de síntese, decomposição, simples troca e dupla troca:
I) 2 NaNO3 → 2 NaNO2 + O2
II) 2Mg + O2 → 2MgO
III) BaCl2 + K2SO4 → BaSO4 + 2 KCl
IV) Mn + Pb(NO3)2 → Mn(NO3)2 + Pb
a) II, I, IV, III
b) II, I, III, IV
c) I, II, IV, III
d) III, IV, II, I
e) IV, III, II, I
a) II, I, IV, III

Questão 6
Para estudar mais, leia Reações químicas e Transformações químicas.
VIEIRA, Natália. Exercício sobre reações químicas (com gabarito resolvido). Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/exercicio-sobre-reacoes-quimicas-com-gabarito-resolvido/. Acesso em:


