Exercícios sobre átomos (com gabarito resolvido)
Teste seus conhecimentos com as questões a seguir sobre átomos. Confira os comentários após o gabarito para tirar suas dúvidas sobre o tema.
Questão 1
Atomística é a área da Química que estuda os átomos. O átomo é a unidade fundamental da matéria e a estrutura que identifica os elementos químicos.
Sobre os átomos é correto afirmar que
I. Embora a palavra átomo tenha origem grega e signifique indivisível, hoje sabemos que o átomo é formado por partículas ainda menores.
II. Átomos no estado fundamental são carregados negativamente.
III. Um conjunto de átomos com o mesmo número de prótons representa um elemento químico.
Estão corretas as afirmativas:
a) I e II
b) II e III
c) I e III
d) Todas as alternativas
Questão 2
O núcleo de um átomo pode ser definido como
a) Uma pequena e densa região central, que é responsável por praticamente toda a massa do átomo.
b) Uma grande região carregada positivamente, pois é formada apenas por prótons.
c) Uma região pequena e neutra, pois é constituída apenas das partículas chamadas de nêutrons.
d) Uma região do átomo sem carga, visto que as partículas positivas e negativas se anulam neste espaço.
Questão 3
Os estudos sobre a radioatividade levaram o cientista neozelandês Ernest Rutherford a identificar uma região do átomo constituída de grandes espaços vazios chamada de
a) Núcleo
b) Orbital
c) Eletrosfera
d) Camada elétrica
Questão 4
Preencha a tabela a seguir com as informações sobre as partículas subatômicas.
| Partícula | Símbolo |
Carga elétrica |
Massa relativa |
Localização |
|---|---|---|---|---|
| próton | p | 1 | ||
| n | 0 | núcleo | ||
| elétron | -1 | 1/1836 |
Questão 5
As partículas que permitem fazer a distinção entre os átomos dos elementos químicos e que são responsáveis pela ordem com que eles estão dispostos na Tabela Periódica são:
a) Prótons
b) Elétrons
c) Nêutrons
Questão 6
As ligações químicas são resultado da união de átomos de elementos químicos por meio da transferência ou compartilhamento de:
a) Prótons
b) Elétrons
c) Nêutrons
Questão 7
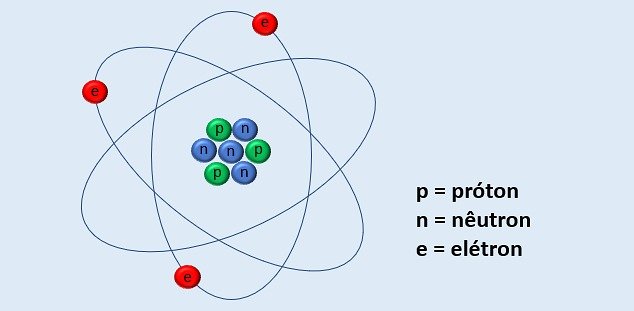
O número atômico e o número de massa do átomo representado na imagem é, respectivamente:
a) 3 e 3
b) 3 e 7
c) 6 e 7
d) 7 e 10
Questão 8
O sódio é um metal que está presente no primeiro grupo da tabela periódica. O átomo desse elemento pode ser representado por 11Na23. O número de prótons, elétrons e nêutrons desse elemento é, respectivamente:
a) 23, 23 e 11
b) 11, 23 e 12
c) 12, 12 e 11
d) 11, 11 e 12
Questão 9
Fissão nuclear corresponde ao processo de divisão do núcleo de um átomo instável e que origina outros átomos. Nesse tipo de reação, uma grande quantidade de energia é liberada e aplicada principalmente em usinas nucleares, que convertem a energia nuclear em energia elétrica.
Por exemplo, quando um átomo de urânio (U) é atingido por um nêutron, a fissão faz surgir dois núcleos menores, que correspondem aos átomos de criptônio (Kr) e bário (Ba), e também libera três nêutrons que bombardeiam outros núcleos numa reação em cadeia.
Se o número atômico do urânio é 92 e o do bário é 56, qual o número atômico do criptônio?
a) 32
b) 36
c) 44
d) 46
Questão 10
Relacione corretamente o cientista (coluna 1) e o respectivo modelo atômico proposto (coluna 2).
Coluna 1
I. Dalton
II. Thomson
III. Rutherford
IV. Bohr
Coluna 2
( ) Átomos apresentam um núcleo positivo e elétrons que se movimentam em camadas circulares de energia definida.
( ) Átomos são esferas positivas com partículas de carga negativa distribuídas na superfície.
( ) Átomos são formados por uma região central e de carga positiva, chamada de núcleo, e uma região externa de carga negativa chamada de eletrosfera.
( ) Átomos são partículas minúsculas indivisíveis, esféricas, maciças e indestrutíveis.
A sequência correta é:
a) I, II, III, IV.
b) III, II, IV, I.
c) II, III, I, IV.
d) IV, II, III, I.
Questão 11
Analise as afirmativas a seguir.
I. Os prótons, partículas carregadas positivamente, estão numa pequena região central do átomo, o núcleo, e ao seu redor movem-se os elétrons.
II. Os estudos sobre a natureza elétrica da matéria desencadearam a descoberta de partículas carregadas negativamente, os elétrons.
III. Os elétrons movem-se em camadas circulares ao redor do núcleo, que apresentam valores de energia específicos.
IV. Os átomos são partículas minúsculas, esféricas e indivisíveis. Átomos de elementos químicos distintos diferem-se pela massa e tamanho.
A sequência correta que corresponde à evolução dos modelos atômicos é:
a) I, II, III e IV
b) III, IV, II e I
c) IV, II, I e III
d) II, III, IV e I
Questão 12
O modelo atômico quântico é o mais moderno e complexo proposto para explicar a estrutura do átomo. Segundo a teoria, é correto afirmar que
a) Não é possível determinar a posição exata de um elétron, pois as partículas se movem num espaço tridimensional formando uma nuvem eletrônica ao redor do núcleo.
b) De acordo com a mecânica quântica, as três principais partículas subatômicas, prótons, nêutrons e elétrons, apresentam carga.
c) Os números quânticos são capazes de identificar a posição dos prótons em um átomo.
d) Os nêutrons são partículas-onda em uma trajetória elíptica na parte central do átomo.
Confira mais questões sobre modelos atômicos com resolução comentada.
Questão 13
Para mais exercícios:
Exercícios sobre estrutura atômica (com gabarito comentado)
Exercícios sobre semelhanças atômicas (com respostas explicadas)
Exercícios sobre a tabela periódica (com gabarito comentado)
VIEIRA, Natália. Exercícios sobre átomos (com gabarito resolvido). Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/exercicios-sobre-atomos/. Acesso em:


