Destilação
A destilação é um método de separação de misturas homogêneas, ou seja, quando os componentes estão em uma única fase.
Existem dois tipos de destilação. A destilação simples é utilizada na separação sólido-líquido e a destilação fracionada em uma mistura de líquidos miscíveis entre si.
Para conseguir isolar um determinado componente de uma mistura é necessário modificar uma variável. No caso da destilação, a separação ocorre pela mudança de temperatura para que o componente de interesse mude de estado físico.
A propriedade das substâncias utilizada neste processo é o ponto de ebulição, ou seja, temperatura em que ocorre a mudança do estado líquido para o gasoso.
Processo de destilação
O processo de destilação consiste em fornecer calor a uma mistura até que o ponto de ebulição do componente de interesse seja atingido e ele passe para o estado gasoso, separando-se dos demais.
Após isso, o gás passa por uma coluna de resfriamento, onde será retirado calor da substância até que atinja seu ponto de fusão e, assim, retorne para o estado líquido. Esse material é direcionado para outro recipiente.
Destilação simples
Para separar uma mistura homogênea de sólido dissolvido em líquido é utilizado a destilação simples.
Na imagem abaixo podemos ver os equipamentos básicos para o processo de separação.
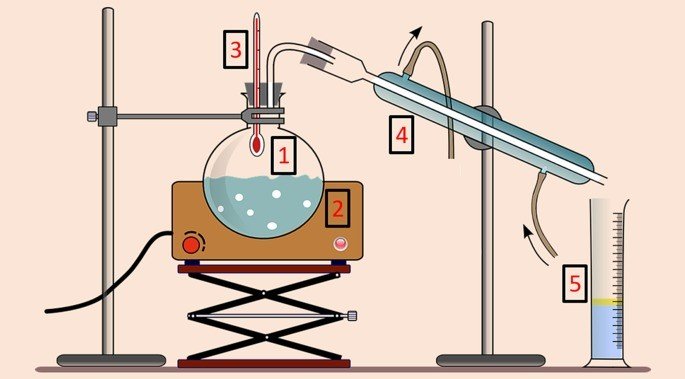
São eles:
- Balão de destilação (1), que contém a mistura;
- Manta aquecedora (2), que fornece calor à mistura;
- Termômetro (3), para acompanhar a mudança de temperatura;
- Condensador (4), para resfriar o componente evaporado e
- Proveta (5), para recolher o componente separado no estado líquido.
Este processo pode ser utilizado, por exemplo, para separar o cloreto de sódio (NaCl), conhecido como sal de cozinha, e água. O sal tem ponto de ebulição 1465 °C e solubiliza-se em água formando uma mistura homogênea.
Como a água apresenta ponto de ebulição de 100 ºC, ela facilmente passa para o estado gasoso e é separada da mistura, enquanto o sal cristaliza-se e mantém-se em estado sólido no recipiente.
O vapor de água sai pela parte superior do balão de destilação e passa por um condensador. Nas paredes desse equipamento circula água fria ou gelada. A troca de calor entre os fluidos faz com que o componente separado da mistura perca calor e volte ao estado líquido para ser recolhido em outro recipiente. Este líquido recebe o nome de destilado.
Destilação fracionada
Para separar uma mistura homogênea de líquidos miscíveis entre si e com uma grande diferença entre as temperaturas de ebulição é utilizada a destilação fracionada.
Este método é fracionado porque os componentes são separados da mistura em ordem crescente do ponto de ebulição, ou seja, iniciando com o de menor até o que requer maior temperatura para mudar de fase.
Na imagem a seguir, há os equipamentos utilizados para realização do método.
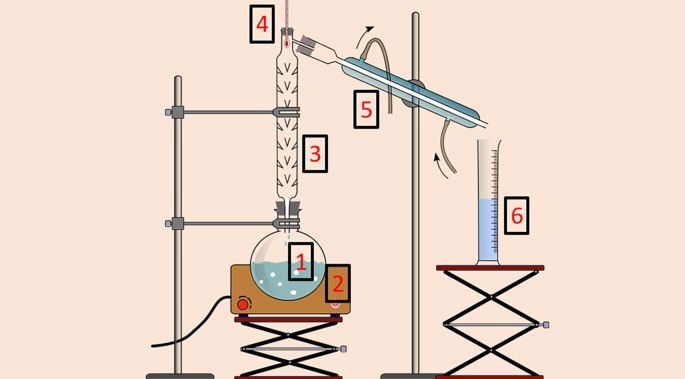
Assim como na destilação simples, balão de destilação (1), manta aquecedora (2), termômetro (4), condensador (5) e proveta (6) são utilizados. Entretanto, a coluna de destilação ou de fracionamento (3) é o equipamento que permite a separação de acordo com a temperatura.
A coluna de destilação apresenta em seu interior uma série de obstáculos para impedir que todos os componentes da mistura volatilizem ao mesmo tempo.
Este processo é amplamente utilizado para separar as frações do petróleo, que é uma mistura de hidrocarbonetos. Alguns dos componentes do petróleo e seus respectivos pontos de ebulição (PE) são: butano (PE 20 ºC), gasolina (PE 150 ºC) e querosene (PE 300 ºC).
Através da destilação fracionada, o butano é o primeiro componente separado, pois tem o menor ponto de ebulição, em seguida a gasolina, com ponto de ebulição intermediário, e por fim o querosene.
Saiba mais sobre a destilação fracionada.
Aplicações da destilação
A destilação é amplamente utilizada em indústrias, pois muitas misturas são submetidas a esse processo. As bebidas destiladas, como uísque, aguardente e vodca, são fabricadas utilizando o método.
A indústria petroquímica utiliza a destilação fracionada para o refino do petróleo. As torres de destilação são grandes estruturas confeccionadas para separar as frações deste combustível fóssil.

Exercícios sobre destilação
Questão 1
A destilação é um método de separação baseado em uma propriedade
a) Química
b) Física
c) Biológica
d) Geral da matéria
Questão 2
São exemplos de misturas separadas por destilação, EXCETO
a) água + acetona
b) salmoura
c) água + azeite
d) água do mar
Questão 3
(UFRGS) Um sistema heterogêneo bifásico é formado por três líquidos diferentes A, B e C. Sabe-se que:
A e B são miscíveis entre si;
C é imiscível com A e com B;
A é mais volátil que B.
Com base nessas informações, os métodos mais adequados para separar os três líquidos são:
a) centrifugação e decantação.
b) decantação e fusão fracionada.
c) filtração e centrifugação.
d) filtração e destilação fracionada.
e) decantação e destilação fracionada.
Continue testando seus conhecimentos com exercícios sobre destilação (com gabaritos explicados).
Adquira mais conhecimento com os conteúdos:
Destilação simples e fracionada
BATISTA, Carolina. Destilação. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/destilacao/. Acesso em:


