Estude este conteúdo
em outros formatos:
A Tabela Periódica é um modelo que agrupa todos os elementos químicos conhecidos e suas propriedades. Eles estão organizados em ordem crescente de número atômico (número de prótons).
No total, a nova Tabela Periódica possui 118 elementos químicos (92 naturais e 26 artificiais).
Cada quadrado especifica o nome do elemento químico, seu símbolo e seu número atômico.
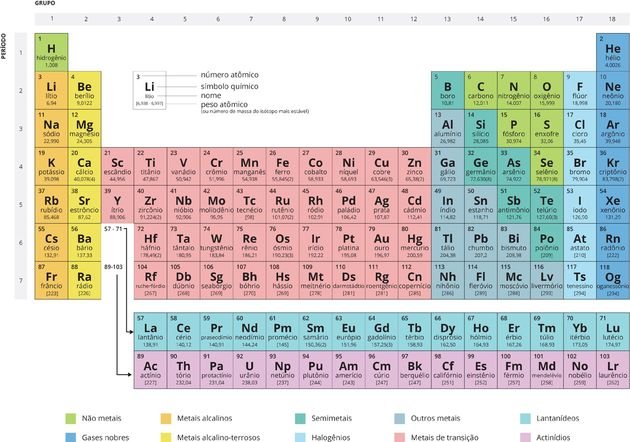
Organização da Tabela Periódica
Os chamados períodos são as linhas horizontais numeradas, que apresentam elementos com o mesmo número de camadas eletrônicas, totalizando sete períodos.
- 1º Período: 2 elementos
- 2º Período: 8 elementos
- 3º Período: 8 elementos
- 4º Período: 18 elementos
- 5º Período: 18 elementos
- 6º Período: 32 elementos
- 7º Período: 32 elementos
Com a organização dos períodos da tabela, algumas linhas horizontais se tornariam muito extensas, por isso, é comum representar a série dos lantanídeos e a série dos actinídeos à parte dos demais.
Os grupos, anteriormente chamados de famílias, são as colunas verticais, onde os elementos possuem o mesmo número de elétrons na camada mais externa, ou seja, na camada de valência.
Ao todo, 18 grupos formam a Tabela Periódica. Muitos elementos destes grupos estão relacionados de acordo com suas propriedades químicas.
- Grupo 1 (Família 1A): Metais Alcalinos (lítio, sódio, potássio, rubídio, césio e frâncio).
- Grupo 2 (Família 2A): Metais Alcalinoterrosos (berílio, magnésio, cálcio, estrôncio, bário e rádio).
- Grupo 13 (Família 3A): Família do Boro (boro, alumínio, gálio, índio, tálio e nihônio).
- Grupo 14 (Família 4A): Família do Carbono (carbono, silício, germânio, estanho, chumbo e fleróvio).
- Grupo 15 (Família 5A): Família do Nitrogênio (nitrogênio, fósforo, arsênio, antimônio, bismuto e moscóvio).
- Grupo 16 (Família 6A): Calcogênios (oxigênio, enxofre, selênio, telúrio, polônio, livermório).
- Grupo 17 (Família 7A): Halogênios (flúor, cloro, bromo, iodo, astato e tenessino).
- Grupo 18 (Família 8A): Gases Nobres (hélio, neônio, argônio, criptônio, xenônio, radônio e oganessônio).
Os elementos de transição, também chamados de metais de transição, ocupam a parte central da tabela:
- Grupo 11 (Família 1B): cobre, prata, ouro e roentgênio.
- Grupo 12 (Família 2B): zinco, cádmio, mercúrio e copernício.
- Grupo 3 (Família 3B): escândio, ítrio, sério de lantanídeos* e actinídeos**.
- Grupo 4 (Família 4B): titânio, zircônio, háfnio e rutherfórdio.
- Grupo 5 (Família 5B): vanádio, nióbio, tântalo e dúbnio.
- Grupo 6 (Família 6B): cromo, molibdênio, tungstênio e seabórgio.
- Grupo 7 (Família 7B): manganês, tecnécio, rênio e bóhrio.
- Grupo 8 (Família 8B): ferro, rutênio, ósmio e hássio.
- Grupo 9 (Família 8B):cobalto, ródio, irídio e meitnério.
- Grupo 10 (Família 8B): níquel, paládio, platina, darmstádio.
*A série de lantanídeos é formada por lantânio, cério, praseodímio, neodímio, promécio, samário, európio, gadolínio, térbio, disprósio, hólmio, érbio, túlio, itérbio e lutécio.
**A série de actinídeos contém os elementos actínio, tório, protactínio, urânio, netúnio, plutônio, amerício, cúrio, berquélio, califórnio, einstéinio, férmio, mendelévio, nobélio e laurêncio.
Por determinação da União Internacional de Química Pura e Aplicada (IUPAC), os grupos são organizados em números de 1 a 18, embora ainda seja comum encontrarmos as famílias descritas por letras e números, como mostrado anteriormente.
Uma importante diferença que o novo sistema apresentado pela IUPAC gerou é que a família 8B corresponde aos grupos 8, 9 e 10 na tabela periódica.
Vale lembrar também que o elemento hidrogênio está posicionado acima dos metais alcalinos apenas devido
à sua configuração eletrônica, mas que não pertence a esse grupo.
Tabela Periódica preto e branco
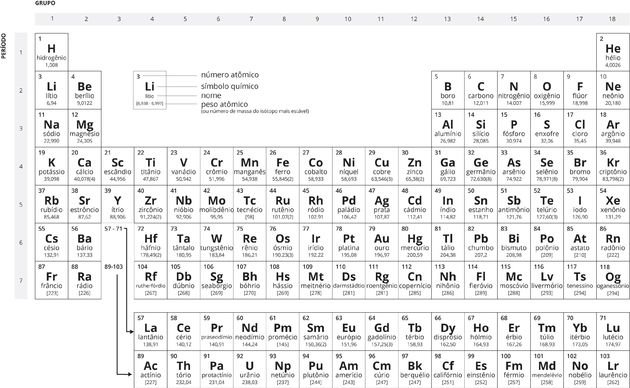
História da Tabela Periódica
A finalidade fundamental de se criar uma tabela era facilitar a classificação, a organização e o agrupamento dos elementos conforme suas propriedades.
Até se chegar ao modelo atual, muitos cientistas criaram tabelas que pudessem demonstrar uma forma de organizar os elementos químicos.
A Tabela Periódica mais completa foi elaborada pelo químico russo Dmitri Mendeleiev (1834-1907), no ano de 1869, em função da massa atômica dos elementos.
Mendeleiev organizou grupos de elementos de acordo com as propriedades semelhantes e deixou espaços vazios para os elementos que ele acreditava que ainda seriam descobertos.
A Tabela Periódica, como a conhecemos atualmente, foi organizada por Henry Moseley, em 1913. Henry Moseley a ordenou pelo número atômico dos elementos químicos, reorganizando a tabela proposta por Mendeleiev.
William Ramsay descobriu os elementos neônio, argônio, criptônio e xenônio. Esses elementos juntamente com hélio e radônio incluíram a família dos gases nobres na Tabela Periódica.
Glenn Seaborg descobriu os elementos transurânicos, do número 94 ao 102. Em 1944 propôs a reconfiguração da Tabela Periódica, colocando a série dos actinídeos abaixo da série dos lantanídeos.
Em 2019, a tabela periódica completou 150 anos. Como forma de reconhecimento de uma das criações mais influentes e importantes da ciência, foi criada uma resolução das Nações Unidas e da UNESCO para que 2019 fosse o Ano Internacional da Tabela Periódica dos Elementos Químicos.
Curiosidades da Tabela Periódica
- A União Internacional de Química Pura e Aplicada (em inglês: International Union of Pure and Applied Chemistry - IUPAC) é uma ONG (Organização não Governamental) dedicada aos estudos e avanços da Química. Mundialmente, o padrão estabelecido para a Tabela Periódica é recomendado pela Organização.
- Há mais de 350 anos, o primeiro elemento químico isolado em laboratório foi o fósforo pelo alquimista alemão Henning Brand.
- O Elemento Plutônio foi descoberto na década de 40, pelo químico estadunidense Glenn Seaborg. Ele descobriu todos os elementos transurânicos e ganhou o Prêmio Nobel em 1951. O elemento 106 recebeu o nome Seabórgio em sua homenagem.
- Em 2016, novos elementos químicos da tabela foram oficializados: Tennessine (Ununséptio), Nihonium (Ununtrio), Moscovium (Ununpêntio) e Oganesson (Ununóctio).
- Os novos elementos químicos sintetizados são chamados de superpesados por conterem em seus núcleos um número elevado de prótons, sendo muito superior aos elementos químicos encontrados na natureza.
Resumo da Tabela Periódica
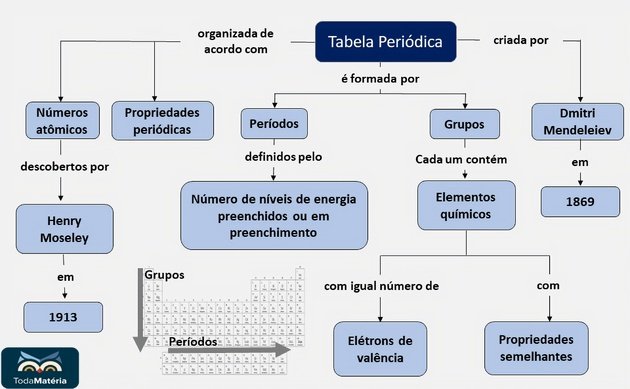
Vídeo sobre a Tabela Periódica
Leia também:
- Famílias da tabela periódica
- História da tabela periódica
- Classificação dos elementos na tabela periódica (tipos e características)
Para praticar:
BATISTA, Carolina. Tabela Periódica. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/tabela-periodica/. Acesso em:

