Modelo atômico de Schrödinger: o que é e as características da teoria
O modelo de Schrödinger, desenvolvido em 1926 pelo físico austríaco Erwin Schrödinger, nos mostra que os elétrons não seguem trajetórias exatas como planetas orbitando o Sol, como sugeria Bohr. Em vez disso, eles estão em regiões chamadas orbitais, onde há uma maior chance de encontrá-los.
Essas regiões são calculadas por uma equação matemática – a equação de Schrödinger – que trata os elétrons como ondas, e não como simples partículas.
A importância dessa nova abordagem é enorme: ela nos permite entender o átomo de forma mais complexa e realista, refletindo a natureza probabilística dos elétrons. Vamos ver como essa ideia nasceu e como ela funciona.
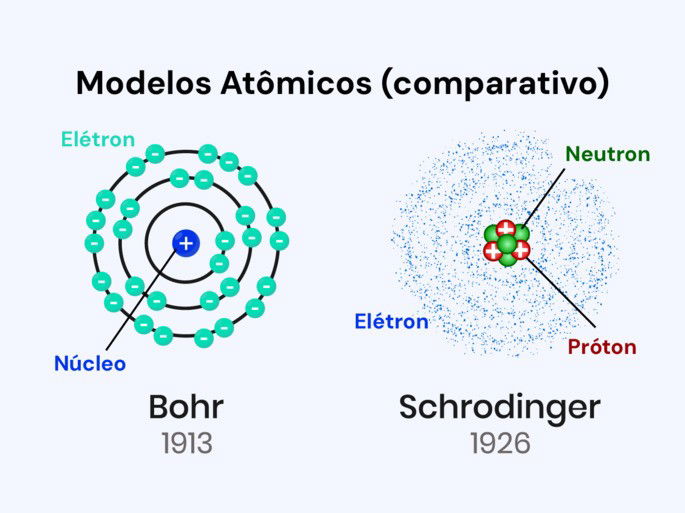
Schrödinger, ao integrar as ideias de De Broglie e Heisenberg, formalizou a teoria de que os elétrons têm comportamento tanto de partículas quanto de ondas. Seus estudos proporcionaram uma explicação mais precisa sobre a energia dos átomos e dos elétrons.
A equação de Schrödinger confirmou o modelo de Bohr para o hidrogênio e também explicou átomos com vários elétrons, algo que Bohr não conseguiu.
Schrödinger não criou um modelo de átomo, mas explicou o comportamento das partículas com cálculos matemáticos. Isso torna sua teoria mais complexa, pois a equação de Schrödinger exige um conhecimento mais avançado de matemática para ser resolvida e compreendida.
Resumo do modelo atômico de Schrödinger
- O modelo de Schrödinger propõe que os elétrons se comportam como ondas, e não como partículas girando em órbitas fixas ao redor do núcleo.
- Equação de Schrödinger: desenvolvida a partir de estudos na mecânica quântica.
- Teorias Fundamentais: a dualidade onda-partícula e o princípio da incerteza foram essenciais para criar a equação.
- Descrição do átomo: o modelo descreve o átomo e os elétrons por meio dessa equação de Schrödinger.
- Movimento dos elétrons: os elétrons não seguem órbitas fixas, mas estão em regiões de probabilidade ao redor do núcleo.
- Orbitais: as regiões onde é mais provável encontrar um elétron são chamadas de orbital.
- Expansão do modelo de Bohr: os estudos de Schrödinger ajudam a entender átomos com mais de um elétron, algo que o modelo de Bohr não explica completamente.
Como Schrödinger criou seu modelo (passo a passo)
Os avanços científicos, como o princípio da incerteza, a dualidade onda-partícula e o efeito fotoelétrico, foram fundamentais para a criação do modelo atômico atual, desenvolvido por Schrödinger.
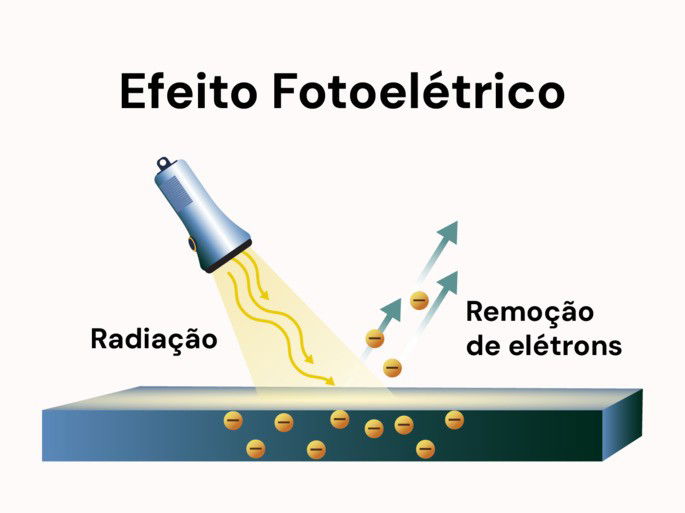
Efeito Fotoelétrico
Estudando a luz como radiação eletromagnética, Einstein descobriu que ela também pode se comportar como uma partícula. O efeito fotoelétrico ocorre quando a luz incide sobre um metal e “arranca” elétrons. A partir disso, Einstein concluiu que a luz é composta por pequenas partículas chamadas fótons, responsáveis por essa interação.
A luz, antes vista apenas como uma onda, também pode se comportar como uma partícula.
Dualidade onda-partícula como inspiração
Em 1924, o físico francês Louis de Broglie propôs que partículas, como os elétrons, podem se comportar tanto como ondas quanto como partículas. Essa descoberta foi revolucionária, pois até então se acreditava que os elétrons eram apenas pequenas esferas girando ao redor do núcleo.
Mas, se o elétron também é uma onda, como podemos saber sua posição exata? Para entender isso, pense em uma corda de violão vibrando: a onda se espalha por toda a corda, tornando difícil determinar um ponto preciso. O mesmo acontece com o elétron, que pode estar em vários lugares ao mesmo tempo, como uma nuvem ao redor do núcleo do átomo.
Schrödinger pegou essa ideia e pensou: “Se o elétron é uma onda, como ele se organiza no átomo?”
O limite do Modelo de Bohr
O modelo de Bohr, de 1913, dizia que os elétrons giravam em órbitas fixas, como trilhos, mas só funcionava bem para o átomo de hidrogênio, que tem um único elétron. Para átomos com mais elétrons, como o carbono ou o oxigênio, ele não explicava tudo. Schrödinger quis ir além e criar algo que funcionasse para todos os átomos.
Princípio da Incerteza de Heisenberg
Na década de 1920, cientistas começaram a perceber que o próprio ato de medir algo pode interferir no resultado. Por exemplo, ao medir a temperatura de um corpo, o termômetro utilizado pode alterá-la levemente, pois ele troca calor com o objeto medido.
Esse efeito é quase imperceptível em objetos grandes, como uma moto ou um carro. No entanto, ao medir partículas muito pequenas, como o elétron, essa interferência se torna significativa. Isso significa que não podemos determinar com precisão tanto a posição quanto a velocidade de um elétron ao mesmo tempo.
Isso não quer dizer que seja impossível fazer medições, mas sim que há um limite natural de precisão. Esse princípio mudou completamente a forma como entendemos o mundo microscópico e foi essencial para o desenvolvimento da mecânica quântica e de tecnologias como os microscópios eletrônicos e os computadores quânticos.
O Princípio da Incerteza afirma que não é possível determinar, ao mesmo tempo, a posição exata e a velocidade de uma partícula, como o elétron.
Para entender melhor, imagine um ventilador. Quando ele está parado, conseguimos ver exatamente onde cada pá está. Mas, quando ele está ligado e girando rapidamente, não conseguimos identificar a posição exata de cada pá, apenas a região onde elas se encontram. Algo parecido acontece com os elétrons no átomo: eles estão sempre em movimento na eletrosfera, o que dificulta determinar sua posição e velocidade ao mesmo tempo.
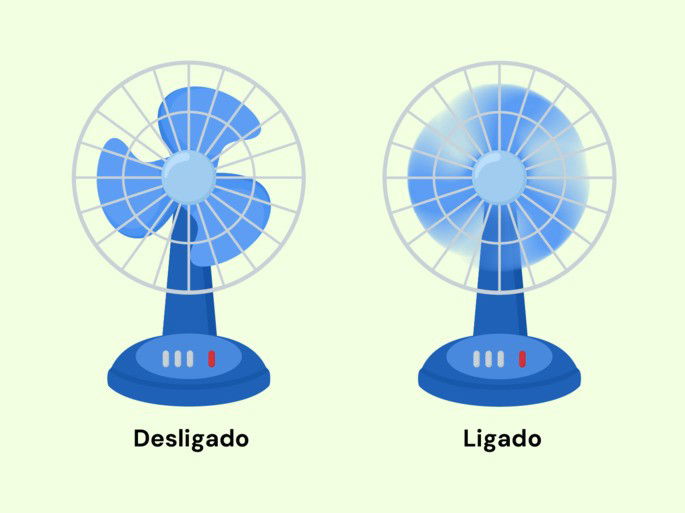
Esse princípio mostra que não podemos definir a trajetória exata de um elétron como fazemos com objetos grandes. Em vez disso, podemos apenas calcular a probabilidade de encontrá-lo em determinada região. Isso mudou a forma como entendemos a estrutura atômica e foi essencial para o desenvolvimento da mecânica quântica.
A Equação de Schrödinger
Em 1926, Schrödinger juntou essas ideias e criou sua famosa equação. Ela descreve o elétron como uma onda e calcula a probabilidade de encontrá-lo em diferentes pontos ao redor do núcleo. Ele testou essa equação com o átomo de hidrogênio, e os resultados bateram com os espectros de luz emitidos por esse átomo, já observados em experimentos.
Características do modelo de Schrödinger
Elétrons como ondas
O modelo vê os elétrons como ondas, não como partículas em trajetórias fixas. A equação de Schrödinger calcula a função de onda (chamada Ψ), que mostra onde o elétron tem mais chance de estar.
Orbitais, não órbitas
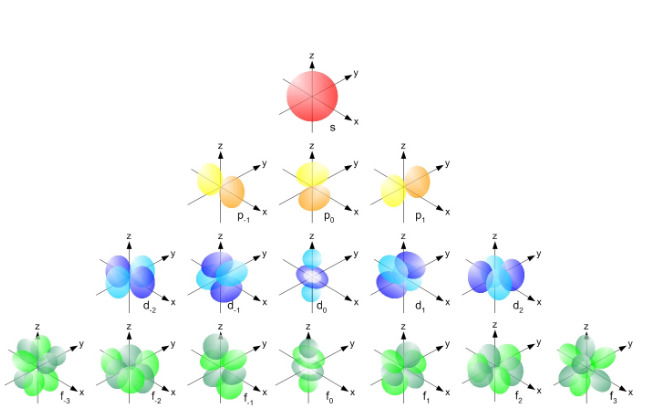
Diferente das órbitas redondas de Bohr, os orbitais são regiões de probabilidade. Eles têm formas variadas:
- Orbital s: Uma esfera ao redor do núcleo.
- Orbital p: Parece um haltere, com dois lados.
- Orbitais d e f: Formas mais complexas, como trevos ou anéis.
Probabilidade, não certeza
Não sabemos o caminho exato do elétron, só as áreas onde ele provavelmente está. Isso reflete o Princípio da Incerteza.
Números quânticos
Cada elétron é descrito por quatro números quânticos, que dizem seu nível de energia, tipo de orbital, orientação e spin (uma espécie de rotação).
O que é o orbital
Orbital é a região onde é mais provável encontrar um elétron.
É provável achar o elétron em pontos internos à figura delimitada pelo desenho e improvável em pontos externos. É importante salientar que o elétron não se movimenta em cima das linhas que delimitam esses desenhos; elas só nos são úteis para representar a forma do orbital.
O modelo de Schrödinger e as implicações para a química moderna
Entender as ligações químicas
Os orbitais mostram como os elétrons se organizam, explicando por que alguns átomos se juntam e outros não. Por exemplo, o oxigênio forma moléculas como H₂O porque seus orbitais p têm espaço para compartilhar elétrons.
Base da tabela periódica
A tabela periódica reflete os orbitais sendo preenchidos. Cada período (linha) é um nível de energia, e os blocos (s, p, d, f) mostram os tipos de orbitais ocupados.
Química moderna e tecnologia
Com a equação de Schrödinger, podemos simular moléculas em computadores, prever reações e criar materiais novos, como plásticos ou remédios. Ele também explica tecnologias como semicondutores e lasers.
Continue estudando sobre os modelos atômicos:
- Modelos atômicos: quais são e qual é o atual
- Evolução dos modelos atômicos
- Modelo Atômico de Dalton
- Modelo Atômico de Bohr
- Modelo Atômico de Rutherford
- Modelo Atômico de Thomson
- Exercício sobre modelos atômicos (com respostas explicadas)
Referências Bibliográficas
BROWN, Theodore L. et al. Química: a ciência central. 9.ed. São Paulo: Prentice Hall, 2005.
FELTRE, R; YOSHINAGA, S. Atomística – 1ª Ed. – São Paulo: Moderna, 1970. p. 138 – 152.
VIEIRA, Natália. Modelo atômico de Schrödinger: o que é e as características da teoria. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/modelo-atomico-de-schrodinger-o-que-e-e-as-caracteristicas-da-teoria/. Acesso em:


